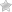Вирус Эпштейна-Барр, поражающий молодую возрастную прослойку населения, является причиной лимфопролиферативных заболеваний, протекающих в острой форме с переходом в хронический процесс.
Вирус определяется у 95% людей и считается непосредственной причиной инфекционного мононуклеоза – первичного проявления заражения.
Дальнейшее развитие событий полностью определяется возможностями иммунитета и включает как бессимптомное носительство, так и злокачественные лимфоидные новообразования.
Причины и патогенез
Вирус Эпштейна-Барр включен в семейство гаммавирусов, которые обладают сродством к лимфоидной ткани. Поражая В-лимфоциты, герпес 4 типа ведет к иммунодефициту и злокачественному перерождению клеток в результате пожизненной персистенции.
Вирус Эпштейна-Барр с организмом хозяина взаимодействует в нескольких формах:
- острой первичной инфекции или обострения;
- хронической (более 6 месяцев);
- носительство (бессимптомное течение);
- в форме медленной вирусной инфекции.
- Медленная инфекция описывается длительной инкубацией (месяцы, годы) с последующей постепенной прогрессией, формированием тяжелых последствий и смерти.
- Данный процесс характерен для лиц с иммунодефицитом, именно при медленной инфекции развивается злокачественное перерождение лимфоидной ткани.
- Уникальной способностью вируса, как и других герпесвирусов, считается способность к пожизненной персистенции и латенции в пораженных клетках.
- Персистенция Epstein Barr представляет собой цикличное, непрерывное деление вируса в В-лимфоцитах, что и считается этиологическим фактором формирования инфекционного процесса.
- Латенция является бессимптомной разновидностью течения инфекции, она проявляется только положительными анализами на антитела G, количество их невысокое.
В период латенции ДНК Epstein Barr в крови методом ПЦР даст отрицательный результат. Это обусловлено нарушением полноценного цикла репродукции вируса, в результате чего он находится в В-лимфоцитах в форме субвирусных структур.
Первичная инфекция и реактивация вируса Эпштейна-Барр отличаются по своим клиническим формам:
- Первичное инфицирование чаще всего протекает в форме инфекционного мононуклеоза, а также иногда встречается саркома мышц, воспаление мозга (энцефалит) и лимфоидная интерстициальная пневмония новорожденных.
- Реактивация может иметь вид гепатита, лимфомы Беркитта, рака глотки и носа, лейкоплакии языка, синдрома хронической усталости, лимфопролиферативного синдрома, аутоиммунных заболеваний, В-клеточной лимфомы.
Epstein Barr virus способен поражать только человека. Соответственно, заразиться герпесом 4 типа можно только от больных людей или носителей.
Вирус Эпштейн-Барр имеет различные способы передачи. Механизмы заражения:
- Артифициальный или искусственный, например, при переливании крови, трансплантации органов, при оказании любых медицинских услуг и нарушении санитарно-противоэпидемического режима.
- Контактно-бытовой посредством предметов быта.
- Алиментарный при грудном вскармливании.
- Аспирационный – путем вдыхания аэрозоля слюны, носоглоточной слизи.
- Половой.
- Вертикальный (от матери к плоду).
Факторы передачи Эпштейна-Барр:
- кровь;
- слюна;
- мокрота;
- женское молоко;
- сперма;
- отделяемое влагалища;
- моча;
- органы и ткани донора.
- Причины возникновения рецидива инфекции в виде опухолей или аутоиммунного процесса обусловлены нарушением иммунного ответа по различным причинам.
- Примечательно, что реактивация ВЭБ в виде лимфомы Беркитта в большей степени характерна для южных стран с жарким климатом, а в средней полосе с умеренным климатом регистрируется редко.
- Вирус Эпштейна-Барр распространен по всему миру в человеческой популяции и поражено им практически 100% населения планеты.
Первичное инфицирование наступает чаще всего к 3 годам и связано с началом посещения детских организованных коллективов. Для заражения ВЭБ необходим тесный контакт.
Симптомы инфицирования Эпштейна-Барр
Симптоматика вируса Эпштейна-Барр при первом заражении проявляется в виде инфекционного мононуклеоза. Ведущим звеном патогенеза является изменение картины крови, а именно нарушение свойств В-лимфоцитов и моноцитов, снижение активности Т-лимфоцитов. В-лимфоциты, внутри которых паразитирует ВЭБ, интенсивно делятся и образуют весомый пул измененных клеток.
Инфицированные вирусом моноциты образуют, так называемые атипичные мононуклеары, определяющиеся в крови спустя 7-10 дней после первых симптомов Эпштейна-Барр.
Действие ВЭБ направлено и на клеточное звено иммунитета. Т-лимфоциты теряют способность нейтрализовать вирусы, а синтез интерферонов претерпевает дисбаланс.
Инфекционный мононуклеоз может быть врожденным и приобретенным. В зависимости от клинической формы выделяют:
- типичное течение;
- атипичную форму.
Кроме того, заболевание может протекать в виде легкой формы, среднетяжелой и тяжелой. Поэтому симптомы и лечение мононуклеоза будут взаимосвязаны.
Инкубация инфекции длится от 4 недель до 1,5 месяцев. Первый признак герпеса 4 типа обусловлен набором острых симптомов:
- подъем температуры тела до очень высоких значений, максимальные цифры отмечаются на 2-3 день болезни;
- увеличение в размерах лимфатических узлов задней и боковой шейной группы, а также подмышечных, паховых и других. Шея приобретает «фестончатый» вид;
- острое воспаление миндалин и аденоидов, на миндалинах появляется белый налет;
- выраженная заложенность носа, отек носоглотки, храп во сне;
- к 10 дню заболевания увеличивается печень, что сопровождается легкой желтухой;
- боли в животе, дискомфорт;
- на протяжении нескольких дней сохраняется сыпь на теле.
После выздоровления о первичной инфекции Эпштейна-Барр около полугода сохраняются увеличенные лимфоузлы.
Важно!
Помимо первичного мононуклеоза, различают и хроническую форму, развивающуюся у 20% лиц, перенесших острый процесс.
Симптомы вируса Эпштейна-Барр при хроническом мононуклеозе дифференцируют у взрослых и у детей.
Признаки хронизации процесса у взрослых:
- симптомы интоксикации: не проходящая усталость и слабость после острого процесса, головные боли, возвращающаяся субфебрильная температура;
- лимфаденопатия;
- увеличение размеров печени и селезенки;
- тонзиллит;
- воспаление аденоидов;
- воспалительные процессы органа зрения;
- патологии ЦНС.
Синдромы хронизации ВЭБ у детей:
- аденоидит;
- хронический тонзиллит;
- повторяющийся субфебрилитет;
- сохранение увеличения печени и селезенки;
- повторные, затяжные ОРВИ;
- слабость, усталость, отставание в учебе, вялость.
Помимо перечисленного, могут болеть суставы и сердце.
К осложнениям вируса Эпштейна-Барр относят:
- гепатит;
- менингит и энцефалит;
- миокардит;
- пневмония;
- снижение количества тромбоцитов;
- гемолитическая анемия;
- почечная, печеночная недостаточность;
- синдром Рея;
- полирадикулоневропатия.
Ассоциированные с вирусом Эпштейна-Барр опухоли
При длительном хроническом течении первичной ВЭБ-инфекции, а также на фоне иммунодефицита при других патологиях и состояниях, вирус может привести к злокачественным новообразованиям. Чаще всего диагностируются лимфома Беркитта, рак носоглотки.
Лимфома описывается повышением температуры, ростом опухоли в районе верхней челюсти, которая прорастает мягкие ткани и кости, метастазируя.
Назофарингеальная карцинома, как и лимфома, чаще всего описывается в южных странах. Опухоль довольно быстро растет, прорастает носовую кость и кости черепа, дает метастазы в лимфоузлы.
Диагностика ВЭБ
При появлении типичных для мононуклеоза симптомов назначают кровь на анализы на антитела к вирусу, ДНК ВЭБ, а также мазки слюны на ДНК (методом ПЦР).
В зависимости от давности инфицирования и стадии инфекционного процесса, результаты на антитела будут различными:
- В конце первой недели обнаруживают IgM к антигену VCA (капсидному). Через две недели и более фиксируют положительные IgG к этому антигену, а также IgG к ЕА – к оболочке.
- На поздних стадия острого процесса положительными становятся IgG к VCA, ЕА, и к внутреннему белку (EBNA).
- При хроническом мононуклеозе отмечаются положительные IgG к VCA, ЕА.
- Реактивация ВЭБ описывается положительными антителами ко всем антигенам.
- В общем анализе крови отмечают лейкоцитоз умеренного характера, лимфоцитоз (за счет роста популяции В-лимфоцитов), моноцитоз, и увеличение атипичных мононуклеаров более 10%.
- Острый процесс характеризуется положительными анализами ПЦР на ДНК вируса в слюне, крови, моче.
- Всем пациентам проводят УЗИ брюшной полости, биохимический анализ крови, в котором отмечают незначительное повышение печеночных трансаминаз и билирубина.
Дифференцируют заболевание с цитомегаловирусным мононуклеозоподобным синдромом, ВИЧ, токсоплазмозом, аденовирусом, стрептококковой ангиной, дифтерией. Реактивацию ВЭБ принято дифференцировать с острым лимфобластным лейкозом, лимфогранулематозом.
Лечение
Лечение зависит от клинической картины, тяжести течения заболевания.
Легкие формы, которые не сопровождаются фебрильной лихорадкой, увеличением печени, протекают без осложнений и выраженного воспаления лимфоидного кольца полости рта принято лечить в домашних условиях. Специфическая терапия при этом не требуется. Назначаются препараты для снижения температуры, обильное питье и диета.
Инфекция средней степени тяжести и тяжелые формы подразумевают лечение Эпштейна-Барр в стационаре с целью предупреждения пневмонии, энцефалита и других осложнений.
Лечение вируса Эпштейна-Барр включает блоки:
- Этиотропная терапия. При всех формах инфекции включают препараты интерферона, так как вирус подавляет выработку собственного. В возрастных дозировках каждый день используют свечи, например, Кипферон, Виферон на протяжении 14 дней. Далее, через день в течение квартала. При хронической форме – до 9 месяцев. Также принимают индукторы интерферона (Амиксин, Арбидол, Циклоферон).
- Синдромальная терапия. Короткий курс гормонов глюкокортикоидов используют при невозможности носового дыхания. Фебрильная лихорадка, интоксикация служат поводом для внутривенных инфузий солевых растворов. Для профилактики или лечения бактериальных осложнений назначают антибиотики из группы макролидов, цефалоспоринов, так как амоксициллины и ВЭБ обеспечивают появление сыпи.
- Сопроводительный блок включает витамины группы В, А, Е, С.
Важно!
Диета при герпесе 4 типа обязательна к соблюдению ввиду поражения печени вирусом.
В процессе лечения вируса Эпштейна-Барр исключаются из рациона сладости, особенно шоколад, кофе, какао, кислые продукты, жареные блюда, цельное молоко, приправы.
Алкоголь запрещается принимать на протяжении минимум полугода, так как вирус довольно длительное время переходит в латентное состояние. Пища должна быть обогащена белком, витаминами.
Разрешается к применению нежирное мясо в протертом виде, тушеные или вареные овощи, каши, мясные суфле, некислый творог, сыр, масло, паровой омлет.
Быстро вылечить герпес 4 типа невозможно. Инфекция медленная и требует длительного лечения.
Пациент считается выздоровевшим, если полностью отсутствует клиника, анализы ПЦР на ДНК вируса Эпштейна-Барр и атипичные мононуклеары отрицательные.
Лечение народными средствами актуально только после выздоровления в рамках профилактики рецидива. Применяют травы, повышающие сопротивляемость организма: женьшень, элеутерококк, аралию, родиолу.
Использовать растительные компоненты для лечения вируса Эпштейна-Барр можно только после согласования с врачом.
Вирус меняет активность иммунитета, а растительные стимуляторы могут спровоцировать аутоиммунные заболевания. У детей данные травы при ВЭБ запрещены к применению.
- В период реконвалесценции необходимо снизить физические нагрузки, исключить вредные пищевые привычки, рационально организовывать режим труда и отдыха.
- Вирус Эпштейна-Барр подрывает активность иммунитета, поэтому период восстановления организма после инфекции подразумевает исключительно здоровый образ жизни.
- врач-инфекционист, Куликовская Наталья Александровна.
Источник: https://pro-herpes.ru/virus-epshtejna-barr/veb.html
Инфекции, вызванные вирусом Эпштейна — Барр
Возбудитель — герпесвирус, тип 4 (ВПГ-4), с двунитевой спирализованной ДНК. Поражает лимфоциты и эпителиальные клетки; инфекция обычно длительная, латентная, с частой реактивацией.
Инфекционный мононуклеоз
Диагностические критерии
Соответствующий клинический синдром.
Серологическая диагностика. См. гетерофильную агглютинацию (реакция Пауля — Буннелля).
Наличие ВЭБ может быть подтверждено биопсией печени путем гибридизации in situ или ПЦР.
ПЦР может определять нуклеиновую кислоту вируса Эпштейна — Барр в тканях недифференцированной назофарингеальной карциномы и для ранней диагностики лимфопролиферативной болезни.
На некоторых стадиях заболевания встречаются признаки умеренного гепатита (например, повышение сывороточных трансаминаз и уробилиногена мочи), но они могут быть преходящими.
Сывороточный билирубин повышается у ^ 30% взрослых и у < 9% детей. В 75% случаев развивается билирубино-ферментная диссоциация (сывороточный билирубин в норме или < 2 мг/дл с умеренным повышением ЩФ, ГГТ, ACT, АЛТ).
Если патологии печени нет, то необходимо искать другой диагноз.
В течение 1-й недели болезни выявляются лейкопения и гранулоцитопения. Позже лейкоциты повышаются (обычно 10000—20 000/мкл) за счет повышения уровня лимфоцитов; пик изменений формируется на 7-10-й день и может оставаться на таком уровне примерно 2 месяца. Повышение числа палочкоядерных лимфоцитов и эозинофилия в > 5% случаев.
- Серологические тесты на сифилис, РА и АЯА могут дать ложно-позитивные результаты.
- Примерно в 50% случаев обнаруживается умеренная тромбоцитопения с нарушением функции тромбоцитов.
- Гемолитическая анемия встречается редко.
Гетерофильно-негативный мононуклеозоподобный синдром может развиваться и при таких инфекционных заболеваниях, как ЦМВ, токсоплазмоз, ВПГ. Атипичные лимфоциты также выявляются при других острых заболеваниях (например, краснуха, розеола, паротит, острый вирусный гепатит, острая стадия ВИЧ, реакции на лекарства).
Гетерофильная агглютинация (реакция Пауля — Буннелля)
Агглютинация эритроцитов овец сывороткой пациентов с инфекционным мононуклеозом (ИМ), вызванным вирусом Эпштейна — Барр (ВЭБ).
Коммерческая агглютинация на слайдах (spot) — это сегодня обычный начальный тест, а реакция теста в пробирках с разведениями используется для подтверждения диагноза; коэффициент Ч/С для spot-теста 92% /> 96% (кроме детей < 4 лет, тогда тест менее чувствительный).
Ложнопозитивный результат может наблюдаться при лейкемии, злокачественной лимфоме, малярии, краснухе, гепатите, карциноме поджелудочной железы, присутствовать по нескольку лет у некоторых лиц без видимого объяснения.
Ложно-положительные результаты возникают примерно в 2% случаев, ложно-отрицательные — у 5—7% взрослых.
Титры 1: 56 могут встречаться у здоровых или пациентов с другими заболеваниями.
Титр > 1: 224 предположительно доказывает наличие ИМ, но может быть обусловлен недавней инъекцией лошадиной (иммунизированной) сыворотки. Поэтому необходим дифференциальный абсорбционный тест с использованием почек морских свинок и антигенов бычьих клеток. См. табл. 15.17.
В реакции абсорбции с морскими свинками титр не бывает < 25% от оригинального значения; часто титр не уменьшается более чем в одном-двух разведениях. Если > 90% агглютинации удаляется адсорбцией, то тест считают отрицательным.
Абсорбция эритроцитами быка берет большинство (90%) или всю овечью агглютинацию и снижает титр; доказательство отсутствия ИМ — редукции титра не происходит.
Гетерофильная агглютинация (ГА) положительна у 60% молодых людей во 2-ю неделю и у 90% в 4-ю неделю после развития клинического ИМ; таким образом, результат может быть отрицательным на фоне положительных гематологических и клинических признаков, а вторая ГА одной-двумя неделями позже может быть положительной. Отрицательной ГА может стать, если все еще присутствуют гематологические признаки заболевания. Низкие титры могут персистировать год.
Если для реакции используют эритроциты лошади, то в 75% случаев результаты могут оставаться позитивными до 12 месяцев.
Гетерофильные антитела обнаруживают только у 30% детей младше 2-летнего возраста, 75% детей 2-4-летнего возраста и в > 90% случаев у более взрослых детей.
Ложно-положительные результаты встречаются очень редко и с относительно низкими титрами.
Восстановление титра гетерофильных антител может развиваться как ответ на другие инфекции (например, вирусные инфекции верхних отделов респираторного тракта).
Иногда результат положительный при наличии других заболеваний (например, лимфома, гепатит, аутоиммунные расстройства [ревматоидный артрит], краснуха).
ГА не специфична для ВЭБ. Титры коррелируют с антителами к ВЭБ, не коррелирует с тяжестью заболевания. Непригодны для оценки хронического заболевания.
ГА почти никогда не бывает положительной у японцев с ИМ. Причина данного факта не выяснена.
Гетерофильно-негативный мононуклеозоподобный синдром может развиваться у 10% пациентов (в основном маленькие дети) с токсоплазмозом, вирусными инфекциями (например, ЦМВ, гепатит, краснуха, острая стадия ВИЧ). Отрицательный результат должен быть подтвержден ВЭБ- специфичными антителами.
Хронический мононуклеозоподобный синдром
Описаны 3 типа данного синдрома, но дискутабельно в качестве заболевания.
Состояние, расцениваемое как острый мононуклеоз, длится > 6 месяцев, характеризуется анормальными титрами антител к ВЭБ, гистологическим доказательством органного поражения (например, пневмонит, гепатит), содержанием ДНК или антигенов ВЭБ.
Истинный хронический мононуклеоз обусловлен ВЭБ в > 90% случаев.
Клиническая картина типичная, с позитивными гетерофильными и серологическими признаками первичной ВЭБ- инфекции, но в 5-7% случаев заболевание может быть обусловлено ЦМВ, в < 1% случаях — Toxoplasma gondii. Реже причиной являются ВИЧ, ВПГ-2, вирусы гепатита, ВВО, аденовирус и лекарства (например, фенитоин, сульфасалазин, дапсон).
Тяжелая хроническая активная ВЭБ-инфекция (очень редко) с очень высоким титром антител и персистирующее тяжелое заболевание (например, панцитопения, агранулоцитоз, хронический гепатит, пневмония); может сосуществовать с истинным хроническим мононуклеозом. Гетерофильная реакция положительна примерно в 10% случаев. Окончательной диагностики не существует.
Посттрансплантационная лимфопролиферативная болезнь
- Спектр ВЭБ-ассоциированных расстройств изменяется от инфекционного мононуклеоза до лимфо- мы вследствие применения иммуносупрессивных лекарств.
- Диагностична биопсия вовлеченных в процесс лимфатических узлов.
- ПЦР для определения вирусной нагрузки в периферической крови и тканях.
Количество < 4000 ко
пий/мл крови — очень высокий показатель и соответствует диагнозу. Серийные измерения для отслеживания течения заболевания; < 200 копий/мл предполагает возникновение посттранс- плантационных лимфопролиферативных заболеваний у пациентов, получающих иммуносулрес- сивную терапию.
Серология бесполезна.
Серологическая диагностика вируса Эпштейна — Барр
Тест на антитела к ВЭБ почти не востребован, поскольку 90% случаев являются гетерофильнопозитивными, а ложно-позитивные результаты редки, кроме того, заболевание, как правило, са- моограничивающееся с относительно легким течением. Анализ полезен в атипичных или тяжелых случаях с отрицательным результатом гетерофильного теста, особенно у маленьких детей или иммунокомпрометированных пациентов.
Примеры титров при гетерофильной агглютинации
IgG-VCA (вирусный капсидный антиген): указывает на перенесенную инфекцию и сформировавшийся иммунитет.
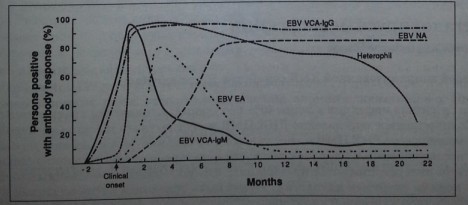
Может присутствовать в начале заболевания, обычно перед появлением клинических симптомов, определяется на ранних стадиях в 100% случаев, в 20% случаев наблюдается 4-кратное повышение титра после визита к врачу.
Снижается в период выздоровления, но определяется многие годы после заболевания, поэтому не является достоверным тестом для диагностики ИМ.
IgM—VC А: определяется в начале заболевания в 100% случаев, высокие титры в сыворотке в течение 1-6 недель развития болезни, затем снижение к 3-й неделе. Исчезают в течение 1-6 месяцев. Сыворотку крови обычно берут слишком поздно для определения антител.
IgM—VCA почти всегда присутствуют при острой ВЭБ-инфекции и являются поэтому специфичными и чувствительными для подтверждения острого ИМ.
Могут быть положительными при других герпесвирусных инфекциях (особенно ЦМВ), следовательно, требуется подтверждение анализом на IgG и ядер- ный антиген вируса Эпштейна — Барр (EBNA).
Анти-D титры ранних антигенов повышаются позже, чем AB-VCA (спустя 3-4 недели после развития инфекции и транзиторно), в период инфекции ИМ и исчезают после выздоровления; сочетание с IgG-VCA предполагает свежую ВЭБ-инфекцию; обнаруживаются только у 70% пациентов с ИМ, вызванным ВЭБ. Высокие титры наблюдаются при назофарингеальной карциноме, вызванной ВЭБ.
Процент лиц с положительным антительным ответом в определенные временные интервалы EBV Я вирус Эпштейн-Барра; VCA — вирусный капсидный антиген; ЕА — ранний антиген; NA — ядерный антиген Источник: Ortho Diagnostic Systems, Raritan, NJ
Антитела класса IgA против капсидного антигена ВЭБ и нейтрализующие антитела против ДНКазы ВЭБ являются предикторами назофарингеальной карциномы.
При первичной ВЭБ-инфекции анти-Л-антитела к раннему антигену редко встречаются в сроки от 2 недель до месяца после инфицирования, могут персистировать в течение года; чаще встречаются в атипичных или затяжных случаях. Не имеющие клинической значимости высокие титры наличествуют при хронической активной ВЭБ-инфекции или лимфоме Беркитта.
Ядерный антиген ВЭБ: антитела к нему появляются в последнюю очередь и редко в острой фазе, на 4-6-й неделе после проявления клинических признаков, повышаются в период реконвалесценции (3-12 месяцев), могут персистировать на многие годы после перенесенной инфекции.
Отсутствие EBNA при наличии IgM—VCA и анти-D — свидетельство свежей инфекции. Появление их в начале заболевания — первичная ВЭБ-инфекция исключается. Появление их после отрицательного результата — доказательство свежей ВЭБ-инфекции.
ТИФА определяет EBNA IgG и IgM одновременно; IgM > IgG при острой инфекции, IgG > IgM после перенесенной ВЭБ- инфекции. Отсутствие EBNA и наличие VCA указывает на острую инфекцию.
- Доказательства острой первичной ВЭБ-инфекции (>1 из перечисленных признаков)
- Острую или первичную ВЭБ-инфекцию исключают при неизменных сывороточных титрах IgG-VCA и EBNA в острой фазе и фазе выздоровления.
- В пользу текущей или свежей инфекции свидетельствуют IgM анти-VCA или IgM/IgG ранние антигены с низким уровнем или отсутствием антител к EBNA.
- Персистенция ранних антигенов и высокий титр IgG-VCA указывают на хроническую ВЭБ- инфекцию
Источник: http://med-slovar.ru/diagnostika-i-issledovaniya/analizy/44-infektsionnye-bolezni/758-infektsii-vyzvannye-virusom-epshtejna-barr
Лабораторная диагностика инфекции, вызванной вирусом Эпштейн-Барр
… по данным различных авторов, в настоящее время до 80-90% населения земного шара инфицировано вирусом Эпштейн-Барр (Тимченко В.Н. и др, 2006). Эпидемиологическое значение вируса Эпштейн-Барр определяется широкой циркуляцией вируса среди населения. В мире ежегодно заражаются от 16 до 800, а в России 40-80 человек на 100 000 населения (Перадзе Х.Д., 2001).
… вирус Эпштейн-Барр — лимфотропный вирус человека, особенностью которого является способность вызывать не гибель клеток, в которых происходит его репродукция, а, напротив, их патологическую пролиферацию. Вирус Эпштейн-Барр является представителем онкогенных ДНК-содержащих вирусов.
Вирус Эпштейн-Барр относится к группе вирусов герпеса (так называемая подгруппа G).
Все герпесвирусы имеют цикл внутриклеточного паразитирования в ядре и цитоплазме пораженной клетке, при этом в ядре накапливаются включения вирусных частиц, что увеличивает размеры как самого ядра, так и клетки в целом (патогенез возникновения гигантских клеток). У человека герпесвирусы могут вызывать самые различные заболевания*.
Уникальным биологическим свойством всех герпесвирусов человека являются (1) тканевой тропизм, (2) способность к персистенции (способность непрерывно или циклично размножаться, то есть реплицироваться, в инфицированных клетках тропных тканей, что создает постоянную угрозу развития инфекционного процесса) и (3) латенции (герпесвирусы сохраняются в нервных ганглиях в течение всей жизни человека).
Вирус Эпштейн-Барр селится в основном в эпителиальных клетках носоглотки и пищеварительного тракта, а также в В-лимфоцитах.
*
Заболевания человека вызываемые герпесвирусами (G-герпесвирусы обладают тропизмом к В- и Т-лимфоцитам, где длительно персистируют):
• Вирус Эпштейн-Барр (вирус герпеса человека 4 типа, ВЭБ, EBV) – инфекционный мононуклеоз, лимфома Беркитта, назофарингеальная карцинома, волосатая лейкоплакия, В-клеточная лимфопролиферация.
• Вирус герпеса человека 6 типа (ВГЧ-6) – В-клеточная лимфома, эритема новорожденных, внезапная экзантема, системные болезни после трансплантации.
• Вирус герпеса человека 7 типа (ВГЧ-7) – эритема новорожденных, синдром хронической усталости.
• Вирус герпеса человека 8 типа (ВГЧ-8) – саркома Капоши у ВИЧ-серонегативных людей; саркома Капоши, ассоциированная с ВИЧ-инфекцией и СПИДом.
Заболевания, обусловленные вирусом Эпштейн-Барр, относятся к СПИД-индикаторным патологиям*. Показана этиологическая роль вируса Эпштейн-Барр при волосатой лейкоплакии – характерного для СПИДа поражения слизистой оболочки полости рта.
Имеются данные о роли вируса Эпштейн-Барр в возникновении энцефалопатии при ВИЧ-инфекции, а также в возникновении ювенильного ревматоидного артрита: вирус Эпштейн-Барр содержит полипептид, присоединяющийся к DR4 и DR1 и вызывающий заболевание.
Иногда вирус Эпштейн-Барр вызывает гепатит.
*
СПИД — индикаторные болезни
Первая группа — это те заболевания, которые присущи только тяжелому иммунодефициту (уровень CD4-лимфоцитов ниже 200/мкл), поэтому они позволяют поставить клинический диагноз даже при отсутствии в крови антител к ВИЧ или ВИЧ-антигенов.
К таким болезням относятся: кандидоз пищевода, трахеи, бронхов; внелегочный криптококкоз; криптоспоридиоз с диареей более 1 мес.; цитомегаловирусные поражения различных органов, помимо печени, селезенки или лимфоузлов у больного старше 1 мес.
; инфекция, обусловленная вирусом простого герпеса, проявляющаяся язвами на коже и слизистых оболочках, которые персистируют более 1 месяца, а также бронхитом, пневмонией или эзофагитом любой продолжительности, поражающим больного в возрасте старше 1 месяца; генерализованная саркома Капоши у больных моложе 60 лет; лимфома головного мозга (первичная) у больных моложе 60 лет; лимфоцитарная интерстициальная пневмония и/или легочная лимфоидная гиперплазия (ЛИП/ЛЛГ комплекс) у детей в возрасте до 12 лет; диссеминированная инфекция, вызванная атипичными микобактериями (микобактерии комплекса М. avium intracellulare) с внелегочной локализацией или локализацией (дополнительно к легким) в коже, шейных лимфатических узлах, лимфатических узлах корней легких; пневмоцистная пневмония; прогрессирующая многоочаговая лейкоэнцефалопатия; токсоплазмоз головного мозга у больного старше 1 месяца.
Вторая группа — это заболевания, которые могут развиваться как на фоне тяжелого иммунодефицита, так и без него. В этих случаях необходимо лабораторное подтверждение диагноза.
К заболеваниям второй группы относятся: бактериальные инфекции, сочетанные или рецидивирующие у детей до 13 лет (более двух случаев за года наблюдения): септицемия, пневмония, менингит, поражения костей или суставов, абсцессы, обусловленные; гемофильными палочками, стрептококками; кокцидиоидомикоз диссеминированный (внелегочная локализация); ВИЧ-энцефалопатия («ВИЧ-деменция», «СПИД-деменция»); гистоплазмоз, диссеминированный с внелегочной локализацией; изоспороз с диареей, персистирующей более 1 мес.; саркома Капоши у людей любого возраста; лимфома головного мозга (первичная) у лиц любого возраста; другие В-клеточные лимфомы (за исключением болезни Ходжкина) или лимфомы неизвестного иммунофенотипа (мелкоклеточные лимфомы типа лимфомы Беркитта и др., иммунобластные саркомы; атипичный микобактериоз диссеминированный с поражением, помимо легких, кожи, шейных или прикорневых лимфоузлов; туберкулез внелегочный (с поражением внутренних органов, помимо легких); сальмонеллезная септицемия рецидивирующая; ВИЧ-дистрофия (истощение, резкое похудание).
Пути передачи вируса Эпштейн-Барр: (1) со слюной, например, при поцелуях; (2) при переливании крови; (3) половым путем.
Распространение вируса через предметы обихода или воздушно-капельным путем маловероятно, но в некоторых руководствах указывается на то, что инфекция все же может передаваться воздушно-капельным путем.
Точных данных о частоте встречаемости ВЭБ-инфекции нет. После первичного инфицирования вирус Эпштейн-Барр остается в организме !!! пожизненно. 15-25% здоровых ВЭБ-позитивных взрослых выделяют вирус из ротоглотки.
В регионах с повышенной частотой инфекционного мононуклеоза отмечается и более высокая частота некоторых форм злокачественных опухолей – как раз тех, что предположительно возникают при непосредственном участии вируса Эпштейн-Барр.
!!! Около 2% детей инфицируется вирусом Эпштейн-Барр во время беременности, и почти 10% — во время родов.
В юношеском возрасте ВЭБ-инфекция может протекать в форме инфекционного мононуклеоза, характерными клиническими признаками которого являются боль в горле, лихорадка, спленомегалия, гепатомегалия и аденопатия. Студенты и военнослужащие являются группами повышенного риска развития инфекционного мононуклеоза.
Транзиторные иммунодефицитные состояния, характерные для больных, перенесших операции по трансплантации органов, больных злокачественными новообразованиями, беременных женщин и лиц преклонного возраста, могут приводить к развитию латентной инфекции. Персистирование ВЭБ-инфекции является этиологическим фактором клинического синдрома, получившего название «хроническая ВЭБ-инфекция» или «хронический мононуклеоз».
Наиболее часто уточнение этиологии заболевания лабораторным методом ПЦР-анализа требуется при поражении органа зрения (увеит, коньюктивит и кератоконьюктиит), центральной нервной системы (серозный энцефалит и менингит) и половых органов (наружные половые органы, цервицит, уретрит), так как не только герпесвирусы, но и довольно большое число других вирусов вызывают острые и рецидивирующие заболевания этих органов. В подобных случаях ошибка в выборе этиопатогенетических препаратов и их доз зачастую приводит к необратимым последствиям. Лабораторный контроль за течением герпесвирусных заболеваний обычно необходим при диссеминации процесса, у беременных женщин и больных с иммунодефицитом различного происхождения.
Учитывая, что вирус Эпштейн-Барр может выделяться в каком-то проценте случаев у здоровых людей, после качественного анализа !!! необходимо провести определение наличия иммуноглобулинов в крови (по иммуноглобулинам G и M), чтобы определить стадию инфекционного процесса.
Наиболее специфичными и чувствительными маркерами острой инфекции являются IgG к раннему антигену (ЕА) и IgM к капсидному комплексу (VCA, или АВК — антиген вирусной капсулы), а маркерами паст-инфекции* – IgG к EBNA-1 (ядерный антиген).
Экспрессия EBNA-1 антигена (ядерного) происходит через 12 – 24 часа после заражения, одновременно или после экспрессии мембранного антигена вируса. Обследование выполненное на первой недели, у 10-15% больных дает отрицательный результат.
IgM-антитела к антигену вирусной капсулы (АВК) диагностически значимы при первичной ВЭБ-инфекции. Ig-анти-АВК антитела обнаруживаются на ранних этапах инфекционного процесса и сохраняются на всю жизнь.
Антитела к ядерному антигену EBNA появляются примерно на 6-8-й неделе и также сохраняются в течение всей жизни. Наличие IgМ-анти-АВК антител и сероконверсия титра антител к ядерному антигену EBNA диагностически значимы при первичной ВЭБ-инфекции.
*Паст-инфекция — появление иммуноглобулинов клacca G к нуклеарному антигену (ЕВNА-1), т.е. маркера давно перенесенной инфекции вирусом Эпштейн-Барр.
- Интерпретация серологических данных:
- • инкубационный период или отсутствие инфицирования: VCA-IgM (ABK IgM) (-); EA-IgG (-);
- • очень ранняя первичная инфекция: VCA-IgM (ABK IgM) (+); EA-IgG (-);
- • ранняя первичная инфекция: VCA-IgM (ABK IgM) (+); EA-IgG (+);
- • поздняя первичная инфекция: VCA-IgM (ABK IgM) (+/-); EA-IgG (+);
- • атипичная первичная инфекция: VCA-IgM (ABK IgM) (+); EA-IgG (-);
- • хроническая инфекция: VCA-IgM (ABK IgM) (-/+); EA-IgG (+);
- • ранняя паст-инфекция: VCA-IgM (ABK IgM) (-); EA-IgG (+);
- • поздняя паст-инфекция: VCA-IgM (ABK IgM) (-); EA-IgG (-);
- • реактивация: VCA-IgM (ABK IgM) (+); EA-IgG (+);
- • атипичная реактивация: VCA-IgM (ABK IgM) (+); EA-IgG (-);
Источник: http://doctorspb.ru/articles.php?article_id=1119
Хроническая инфекция вируса Эпштейна Барр у детей: современные аспекты диагностики и лечения — PDF
1 Приложение к журналу Consilium Medicum педиатрия Репринт 2006 Хроническая инфекция вируса Эпштейна Барр у детей: современные аспекты диагностики и лечения Э.Н.Симованьян, В.Б.Денисенко, А.М.Сарычев, А.В.Григорян Материал опубликован в 2, 2006 г.
2 2 Хроническая инфекция вируса Эпштейна Барр у детей: современные аспекты диагностики и лечения Э.Н.Симованьян, В.Б.Денисенко, А.М.Сарычев, А.В.
Григорян ГОУ ВПО Ростовский государственный университет Федерального агентства по здравоохранению и социальному развитию Инфекция вируса Эпштейна Барр (ЭБВИ) относится к наиболее распространенным инфекционным заболеваниям детского возраста.
В последние годы во всем мире, в том числе в Российской Федерации, отмечается увеличение количества больных ЭБВИ, что связано не только с улучшением качества диагностики, но и с истинным ростом их числа. Заболеваемость острой ЭБВИ (ОЭБВИ) в нашей стране в 2003 г. составила 37,5/100 тыс. детей, что в 2 раза больше по сравнению с 1996 г. [1].
В настоящее время доказана роль вируса Эпштейна Барр (ВЭБ) в развитии ряда злокачественных опухолей (лимфома Беркитта, назофарингеальная карцинома и др.
), аутоиммунных заболеваний (системная красная волчанка, ревматоидный артрит), заболеваний у ВИЧ-инфицированных лиц (лимфоидный интерстициальный пневмонит, волосистая лейкоплакия), хронического гепатита, увеита, патологии нервной системы (энцефалиты, менингиты, миелиты, полирадикулонейропатии), синдрома хронической усталости [2].
В последние годы пристальное внимание ученых привлекает проблема хронической ЭБВИ (ХЭБВИ) в связи с ее не только медицинской, но и социальной значимостью [3 5].
Нашими исследованиями доказано, что длительная репликация ВЭБ и индукция вторичного иммунодефицита приводят к высокой инфекционной заболеваемости, способствуют переходу ребенка в группу часто и длительно болеющих детей [4, 5].
При этом не только нарушаются нормальный рост и развитие больного, снижается качество жизни ребенка и его родителей, но и наносится существенный ущерб бюджету семьи и экономике страны в целом.
Этиология ВЭБ (герпес-вирус 4-го типа) относится к группе g-герпес-вирусов и имеет следующие антигены капсидный антиген (VCA), ранний антиген (EA), ядерный антиген (EBNA) и мембранный антиген (MA) [6 8].
Основными клетками-мишенями для ВЭБ являются В-лимфоциты, однако он может поражать эпителий ротоглотки, протоков слюнных желез, шейки матки, желудочно-кишечного тракта, эндотелий сосудов и иммунокомпетентные клетки Т-лимфоциты (CD3), естественные киллерные клетки (NK-клетки CD16), нейтрофилы, макрофаги. В-лимфоциты имеют специфический рецептор для ВЭБ CD21.
Инфицированные вирусом В-клетки приобретают способность к неограниченной пролиферации (иммортализация, «клеточное бессмертие») и синтезируют большое количество гетерофильных антител (поликлональная активация). Как и все герпес-вирусы, ВЭБ оказывает мощное иммуносупрессирующее действие [9, 10].
Он вызывает нарушение иммунного ответа по клеточному и гуморальному типам, цитокинового статуса, факторов врожденной резистентности. ВЭБ обладает способностью к пожизненной персистенции в организме человека, что связано с индукцией иммунодефицитного состояния (ИДС) и интеграцией ДНК вируса в геном клеток [11, 12].
Эпидемиология Антитела к ВЭБ обнаруживают у 60% детей первых 2 лет жизни и у 80 90% взрослых [13, 14]. Широкому эпидемическому распространению ЭБВИ способствуют большое количество больных и лиц, выделяющих вирус, также многообразие путей передачи вируса, к которым относятся воздушно-капельный, контактно-бытовой, половой, парентеральный и вертикальный.
В нашей стране ОЭБВИ чаще регистрируется в возрастных группах от 1 до 5 лет жизни (43,8%), преимущественно у детей из организованных коллективов. Данные относительно заболеваемости ХЭБВИ отсутствуют. Однако с учетом высокой частоты хронизации заболевания после перенесенной ОЭБВИ (20 37,5%) и существованием первично-хронических форм, количество больных ХЭБВИ, по-видимому, достаточно велико [15]. Патогенез В основе формирования ХЭБВИ лежат действие комплекса неблагоприятных факторов в анте-, интра- и постнатальном периодах, нарушение нейроиммуноэндокринной регуляции, генетическая предрасположенность (рис. 1.). Как показало проведенное нами обследование 120 детей в возрасте от 5 до 14 лет, ХЭБВИ развивается у детей из групп риска. У 86,7% матерей выявлен отягощенный акушерский анамнез хронический эндометрит, гестоз, угроза прерывания беременности и др. В постнатальном периоде к группам риска относятся 83,3% детей: это перинатальное поражение ЦНС, постнатальная патология ЦНС, аномалии конституции, частые инфекции верхних дыхательных путей, патология ЛОР-органов и др. Эти факторы являются причиной формирования вторичного ИДС. Инфицирование ВЭБ приводит к нарушению функциональной активности факторов врожденной резистентности, формированию неполноценного иммунного ответа, прежде всего по клеточному типу (рис. 2). При исследовании цитокинового статуса больных ХЭБВИ выявлено увеличение содержания антагониста интерлейкина-1 (ИЛ-1RA), который ингибирует ИЛ-1-зависимые механизмы инициации иммунного ответа по клеточному типу [16]. Кроме того, имеют место недо- репринт CONSILIUM MEDICUM/приложение
3 Рис. 1. Иммунопатогенез ХЭБВИ у детей.
Неблагоприятные факторы в анте-, интра- и постнатальном периодах Бактериальные, вирусные, грибковые, протозойные инфекции Нарушение нейро-иммуноэндокринной регуляции гомеостаза Вторичное ИДС Генетическая предрасположенность ВЭБ Нарушение презентации и распознавания антигена Нарушение активации иммунокомпетентных клеток Снижение функциональной активности Th1, повышение активности Th2 Недостаточность клеточного иммунного ответа, гиперактивация В-звена, нарушение факторов врожденной резистентности Персистенция ВЭБ в клетках-мишенях Углубление вторичного ИДС Срыв адаптационных механизмов Реактивация ХЭБВИ Неполная ремиссия ХЭБВИ статочная активация иммунокомпетентных клеток (уменьшение количества HLA-DR-лимфоцитов) и повышение их готовности к апоптозу (увеличение экспрессии CD95-рецепторов). В настоящее время установлено, что важную роль в формировании ХЭБВИ играет нарушение регуляции иммунного ответа Т-хелперами 1-го и 2-го типов (Th1, Th2) [17]. Известно, что Th1 секретируют интерферон-g (ИФН-g) и направляют иммунный ответ по клеточному типу. Th2 выделяют ИЛ-4, который стимулирует выработку иммуноглобулинов, прежде всего IgE. У детей с ХЭБВИ зарегистрировано нарушение функциональной активности Th1, что документировано снижением содержания ИФН-g. О недостаточности иммунного ответа по клеточному типу свидетельствует уменьшение общего пула Т- клеток (CD3), количества лимфоцитов с рецепторами к ИЛ-2 (CD25) и NK-клеток (CD16). цитотоксических CD8-лимфоцитов у детей с ХЭБВИ повышено. Однако сохранение маркеров репликации ВЭБ у данной категории пациентов на протяжении длительного времени свидетельствует о нарушении элиминации вируса факторами клеточного иммунного ответа, прежде всего специфическими CD8-лимфоцитами. С другой стороны, при ХЭБВИ повышена функциональная активность Th2, что документировано увеличением содержания ИЛ-4. Отмечается поликлональная активация В-лимфоцитов (CD20), которая сопровождается повышением их числа, а также содержания IgA, IgM, IgG и циркулирующих иммунных комплексов (ЦИК) в крови. У детей с ХЭБВИ возникают нарушения со стороны нейтрофильного звена снижение содержания в крови хемотаксического фактора нейтрофилов (ИЛ-8), активация кислородзависимого метаболизма этих клеток по данным теста восстановления нитросинего тетразолия (НСТ сп.) и редукция его адаптационных возможностей (К ст. НСТ). Нарушения иммунного статуса являются тем патогенетическим фоном, который приводит к длительной персистенции ВЭБ в клетках-мишенях. В условиях ИДС происходит активация условно-патогенной микрофлоры, вирусных и грибковых заболеваний. При анализе микробного пейзажа слизистой оболочки ротоглотки у всех больных ХЭБВИ выявлена условно-патогенная микрофлора (Staphylococcus aureus, Staph. epidermidis, Streptococcus pyogenes, Str. viridans), у 20% грибы рода Candida. У подавляющего большинства (90%) больных заболевание протекает в форме микстинфекции с участием нескольких герпесвирусов (ВЭБ + цитомегаловирус, ВЭБ + вирусы простого герпеса 1-го и 2-го типов). Формирование микстинфекции способствует углублению ИДС, что замыкает «порочный круг» иммунопатогенетических механизмов и приводящих к реактивации ХЭБВИ. В условиях недостаточности специфического иммунного ответа, прежде всего по клеточному типу, не происходит полного подавления репликации ВЭБ. Заболевание переходит в стадию неполной ремиссии. При действии иммуносупрессирующих факторов (углублении ИДС, присоединении микстинфекции и др.) происходит повторная реактивация возбудителя. Классификация Общепринятая классификация ХЭБВИ отсутствует. И.К.Малашенкова и соавт. [18] у взрослых больных выделяют хроническую активную ЭБВИ, генерализованную форму, ВЭБ-ассоциированный гемофагоцитарный синдром и стертую форму заболевания. С учетом того, что ХЭБВИ является одним из вариантов течения ЭБВИ, в практической работе рекомендуем использовать разработанную нами рабочую классификацию заболевания. Она основана на общепринятых патогенетических принципах классификации детских инфекционных болезней и учитывает особенности клинической картины ЭБВИ. Клиническая картина На основании обследования 120 детей с ХЭБВИ разработана синдромальная модель заболевания (табл. 1). Клиническая картина ХЭБВИ включает хронический мононуклеозоподобный синдром генерализованную лимфаденопатию (ГЛАП), хронический тонзиллит, хронический аденоидит, гепатоспленомегалию. У всех больных регистрируется синдром хронической интоксикации, у подавляющего большинства инфекционный 3 CONSILIUM MEDICUM/приложение репринт
4 4 синдром. Все пациенты относятся к группе часто болеющих детей, что связано с длительной репликацией ВЭБ и формированием вторичного иммунодефицита. Острые респираторные инфекции у этих больных возникают с частотой 6 11 раз в год.
Достаточно часто у детей с ХЭБВИ отмечаются изменения со стороны ЦНС в виде гипертензионно-гидроцефального, вегетовисцерального синдромов и синдрома гиперактивности. Кроме того, некоторых пациентов беспокоят проявления кардиального синдрома (боли в сердце, сердцебиение) и артралгии.
Диагностика Диагностика ХЭБВИ основана на комплексном анализе групп риска, клинических симптомов заболевания и данных лабораторного обследования (рис. 3). С помощью иммуноферментного анализа (ИФА) определяют содержание антител класса IgM к VCA-, IgG к EA- и IgG к EBNA-антигенам ВЭБ.
Методом полимеразной цепной реакции (ПЦР) выявляют ДНК ВЭБ в крови, мазках из носоглотки и в других биологических субстратах. В комплекс обследования больных обязательно включают исследование иммунного статуса.
Обследование 120 детей с ХЭБВИ позволило выделить следующие клинико-лабораторные стадии заболевания стадию реактивации (37,5% пациентов), стадию атипичной реактивации (11,2%) и стадию неполной ремиссии (51,3%). Лечение Терапия ХЭБВИ у детей основана на следующих принципах. 1.
Комплексное использование медикаментозных средств этиотропной, патогенетической направленности и немедикаментозных методов лечения. 2. Длительность, непрерывность и преемственность лечения на этапах стационар Ѓ поликлиника Ѓ реабилитационный центр. 3.
Составление индивидуальной программы терапии с учетом возраста пациента, активности инфекционного процесса, клинических, серологических, иммунологических и молекулярно-генетических показателей. С учетом склонности к персистенции и относительной резистентности ВЭБ к противовирусным препаратам необходимо назначение комплексной терапии, воздействующей на все этапы жизненного цикла вируса (табл.
2). Стандарт лечения ХЭБВИ Базисная терапия 1. Охранительный режим 2. Лечебное питание 3. Противовирусные препараты Виростатические препараты изопринозин (инозин пранобекс), аномальные нуклеозиды Препараты ИФН виферон и др. Индукторы ИФН Иммуноглобулины для внутривенного введения по показаниям 4. Локальные антибактериальные препараты 5. Витаминно-минеральные комплексы 6.
Иммунокорригирующая терапия под контролем иммунограммы Интенсификация 1. Пробиотики и пребиотики 2. Препараты метаболической реабилитации 3. Энтеросорбенты 4. Антигистаминные препараты второго поколения по показаниям 5. Гепатопротекторы по показаниям 6. Нейро- и ангиопротекторы по показаниям 7. Кардиотропные препараты по показаниям 8. Ферменты по показаниям 9. Гомеопатические средства 10.
Немедикаментозные методы массаж, лечебная физкультура, иглорефлексотерапия, магнитотерапия, лазеротерапия, электрофорез и др. Симптоматическая терапия 1. При затруднении носового дыхания назальные препараты 2. При сухом кашле противокашлевые препараты; при влажном кашле секретолитические и муколитические препараты 3.
При лихорадке нестероидные противовоспалительные препараты В качестве виростатического препарата для лечения детей с ХЭБВИ мы использовали изопринозин (инозин пранобекс), который обладает рядом достоинств. Изменяя стереохимическую структуру рибосом, он подавляет синтез белков и тормозит репликацию ДНК- и РНК-содержащих вирусов [19, 20]. Кроме того, изопринозин оказы- Рис. 2. Показатели иммунного и цитокинового статусов у детей с ХЭБВИ. Классификация ЭБВИ у детей I. По периоду возникновения Врожденная Приобретенная II. По форме Типичная (инфекционный мононуклеоз) Атипичная: стертая бессимптомная висцеральная III. По тяжести Легкая Среднетяжелая Тяжелая IV. По течению Острая (до 3 мес) Затяжная (3 6 мес) Хроническая (более 6 мес) V. По фазе Активная Неактивная VI. Осложнения: гепатит, разрыв селезенки, синдром Рея, почечная и печеночная недостаточность, серозный менингит и др. VII. Микстинфекция репринт CONSILIUM MEDICUM/приложение
5 Таблица 1. Синдромальная модель ХЭБВИ у детей Синдром Рис. 3. Алгоритм диагностики ХЭБВИ у детей. Число больных абс.
% Лимфопролиферативный ГЛАП Хронический тонзиллит 99 82,5 Хронический аденоидит Гепатомегалия 68 56,7 Спленомегалия 20 16,7 Интоксикационный Инфекционный ,2 Церебральный ,7 Гипертензионно-гидроцефальный Вегетовисцеральный Синдром гиперактивности Кардиальный 40 33,3 Артралгический 29 24,2 Всего Неполная ремиссия ХЭБВИ Ребенок с отягощенным преморбидным фоном Комбинация хронического мононуклеозоподобного, интоксикационного, инфекционного, церебрального, кардиального, артралгического синдромов ИФА, ПЦР, иммунограмма Таблица 2. Механизм противовирусного действия лекарственных препаратов Этап жизненного цикла ВЭБ Внеклеточные вирионы Адсорбция, проникновение Синтез ДНК Синтез вирусных белков Сборка вириона Выход вирионов Группы препаратов Внутривенно иммуноглобулины, изопринозин, ИФН, индукторы ИФН, цитокины, иммуномодуляторы Антиоксиданты Аномальные нуклеозиды Изопринозин, ИФН, индукторы ИФН, препараты метаболической терапии Антиоксиданты Антиоксиданты, ИФН, индукторы ИФН вает иммунокорригирующее действие модулирует иммунный ответ по клеточному типу, стимулирует продукцию антител, цитокинов, ИФН, повышает функциональную активность макрофагов, нейтрофилов и NK-клеток. Изопринозин предохраняет пораженные клетки от поствирусного снижения синтеза белка. В течение многих лет препарат успешно используют для лечения герпес-вирусных инфекций, кори, эпидемического паротита, вирусных гепатитов, папилломавирусной инфекции, подострого склерозирующего панэнцефалита и др. Изопринозин разрешен для применения в педиатрической практике, хорошо переносится больными. Нами обследованы 30 детей с ХЭБВИ в возрасте от 5 до 14 лет. Методом случайной выборки все пациенты разделены на две группы, оказавшиеся сопоставимыми по клинико-лабораторным показателям. Всем больным назначено комплексное лечение по программе (см. выше). У пациентов 1- й группы в качестве противовирусного препарата использован виферон (рекомбинантный ИФНa2b) в форме ректальных свечей по пролонгированной схеме [21]. Больные 2-й группы помимо виферона получали изопринозин в дозе мг/кг в сутки в 3 4 приема внутрь. Проводили 3 курса лечения изопринозином по 10 дней с интервалом 10 дней. Исследование клинических, серологических и иммунологических показателей осуществляли до лечения и через 3 мес после его начала. При анализе результатов монотерапии вифероном у этих пациентов выявлена незначительная динамика клинических симптомов заболевания (табл. 3). У детей, получавших комбинацию изопринозина и виферона, напротив, наблюдалось достоверное уменьшение частоты проявлений лимфопролиферативного синдрома, в том числе ГЛАП, хронического тонзиллита и гепатомегалии. Кроме того, происходило уменьшение частоты интоксикационного и церебрального синдромов (особенно проявлений вегетовисцеральной дисфункции). Следует отметить, что на фоне лечения изопринозином происходило значительное уменьшение частоты инфекционного синдрома. Среднее количество эпизодов острых респираторных инфекций снизилось с 6 11 (7,8±1,5) до 2 4 (2,5±1,4) раз в год (p
Источник: https://docplayer.ru/28075615-Hronicheskaya-infekciya-virusa-epshteyna-barr-u-detey-sovremennye-aspekty-diagnostiki-i-lecheniya.html